2012年,首个基因治疗药物Glybera获欧盟批准,该药物基于腺相关病毒(AAV)载体用于家族性脂蛋白脂酶缺乏(LPLD)成人患者的治疗。
去年,FDA批准的第一个体内基因疗法是Luxturna,同样使用AAV作为递送载体,它被施用于眼睛以治疗罕见的遗传性失明。

1965年,AAV首次被发现为腺病毒样本的污染物。但许多病毒学家认为研究它们是浪费时间,因为它们不会引发任何疾病,而这一事实后来成为基因治疗的最大资产(使其不太可能引起极端的免疫反应)。在当时过去的35年里,科学家们只发现了六种AAV变体,尽管它们看起来很安全,但没有一种特别擅长递送基因。
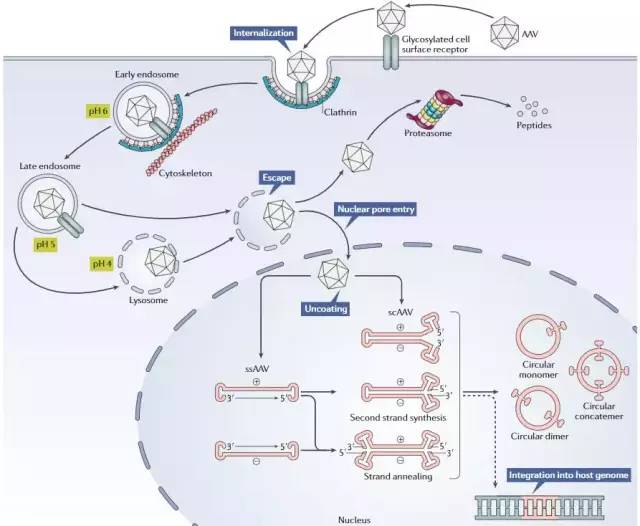
▲ rAAV转导通路(图片来源:Nature Reviews Drug Discovery)
在纯科学的好奇心驱使下,一些研究小组开始了解基本AAV生物学的过程,此时并没有意识到其作为人类基因治疗平台的巨大潜力。在AAV研究的前15-20年中,AAV的几个重要方面被表征,包括其基因组构型和组成、DNA复制和转录、感染潜伏期和病毒粒子组装。这些成果共同促进了野生型AAV2序列成功克隆到质粒中,从而实现了基因研究和整个AAV2基因组测序。早期研究提供了使用AAV作为基因传递载体的基础知识。

▲50年AAV时间线(图片来源:Nature Reviews Drug Discovery )
AVV带来的挑战
基于安全性和治疗性基因容量问题,非病毒递送方法变得越来越普遍。最简单的非病毒基因传递系统如裸DNA、质粒DNA,当直接注射到某些组织,特别是肌肉时,可以产生显著水平的基因表达,但仍然低于用病毒载体实现的基因表达。
目前,病毒载体仍然是基因治疗试验最流行的递送方法,迄今为止,已用于大约三分之二的试验。根据一项2017年的统计,腺病毒是最常用的载体,占所有试验的20.5%,但自2012年(23.3%)以来有所下降。近年来,逆转录病毒载体使用率同样下降(只占试验的17.4%,而2012年为19.7%,2007年为22.8%,2004年为28%),这很大程度上是由于慢病毒载体(约为7.3%,比2012年的2.9%增加)的出现,提高了安全性以及扩大了使用范围。类似的趋势发生在腺相关病毒(AAV)的使用情况,从2012年的4.9%增加到2017年的7.6%。
可负担性已经成为了基于病毒的基因疗法的主要障碍之一
药物产品的可负担性已经成为了基于病毒的基因疗法的主要障碍之一。根据美国知名处方药比价网站GoodRx发布的2019年全球最昂贵药物榜单,两款AAV基因疗法占据了前两名,分别是212.5万美元的Zolgensma和85万美元的Luxturna。今年6月,欧盟批准了Bluebird bio针对重型β地中海贫血的基因疗法Zynteglo(LentiGlobin),其使用慢病毒载体转导CD34+细胞,177万美元的定价使其成为目前全球第二昂贵的药物。
价格主要归因于制造的高成本。要想生产足够的载体用于治疗,需要大量的资源和专业知识以及合适的生产系统。
治疗所需的高剂量也带来了人们对安全性的担忧
威尔逊承认,科学家们仍然不完全理解为什么AAV在一定剂量下会变得有毒,但很明显,如果没有更有效的基因递送工具,高剂量的AAV可能是纠正某些疾病的唯一方法,尤其是肌肉疾病。高剂量还造成了额外的制造障碍和高成本。
这些担忧指导了威尔逊的新公司Passage Bio的战略,该公司专注于研究罕见的遗传神经疾病。该公司临时首席执行官奥比米德•斯奎托(OrbiMed's Squinto)表示:“我们一直在努力选择需要非常、非常低剂量治疗的疾病。”该公司还计划将AAVs直接注射到脑脊液中,这应该比Zolgensma使用的全身注射需要更小的剂量。斯奎托说:“威尔逊在他的职业生涯中不会再冒太多的风险了。在进行人体实验之前,我们将尽可能地了解更多。”
免疫障碍同样存在于当前基因疗法的开发过程中
例如,重组AAV蛋白衣壳、其基因组和转基因的蛋白质产物可以在多个阶段与宿主免疫系统相互作用,对有效基因递送和持久基因表达构成障碍。目前,中和抗体(Nab)筛查和排除血清反应阳性受试者仍然是许多临床研究中的必要步骤。
解决策略
为了避免免疫应答可能导致的问题,研究人员正在测试各种策略,以最小化基因治疗带来的免疫应答。例如,针对免疫特权部位(如眼睛和大脑)的疾病开发基因疗法,一来规避免疫应答带来的风险,二来只需少量施用载体,也避免了临床应用的制造问题。
目前,在遗传性视网膜疾病和中枢神经系统疾病的临床试验中,AAV已经实现了相对的安全性和耐受性。另外,还有证据表明转基因靶向肝脏能诱导免疫耐受。
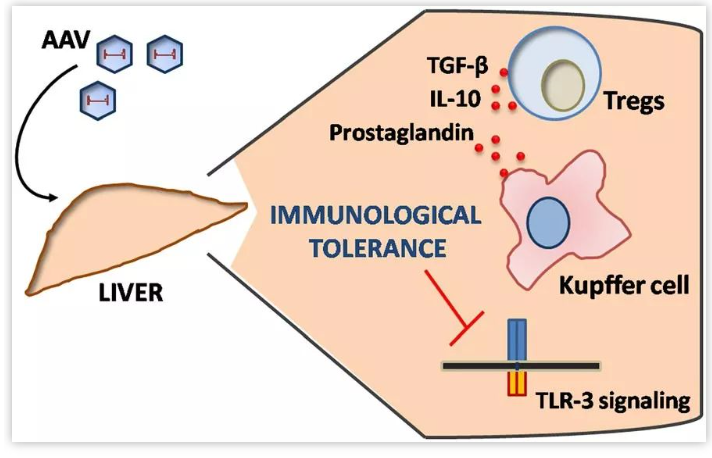
▲AAV介导的基因转移后促成肝脏免疫耐受(图片来源:annualreviews)
基因治疗的安全性得到更多的重视,人们也更加了解可能出现的临床试验中可能出现问题,以及拥有相应的措施。一般的基因治疗,尤其是基于AAV载体的基因治疗,已经十分成熟。基因疗法代表了治愈人类疾病的前沿之一,基因递送载体的革新极大地推动了该领域的发展。挑战仍然存在,使命还远未达成!
「免疫应答」在AAV基因治疗中的挑战与解决策略
基因治疗时代人物威尔逊:20年致力于安全病毒载体的研究,他见证了低沉到华丽回归
华人学者高光坪Nature子刊发文,详述基因治疗明星载体腺相关病毒(AAV)丨医麦猛爆料

